颅内动脉瘤是一种常见的颅内血管疾病,由于先天异常或后天损伤等因素导致局部的血管壁损害, 在血流动力学负荷和其他因素作用下, 逐渐扩张形成的异常膨出。人群中颅内动脉瘤的患病率为2% ~7%,其发生率随年龄增长而增加。
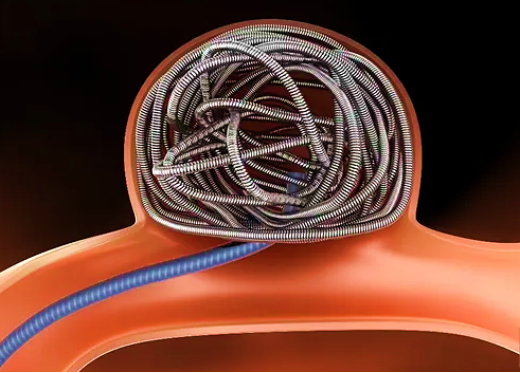
弹簧圈栓塞术是最常见的介入治疗颅内动脉瘤方法,有大宗临床数据证明,大约94%的未破裂动脉瘤可采用单纯弹簧圈栓塞治疗。弹簧圈栓塞术主要是用微导管将弹簧圈送至动脉瘤腔,使动脉瘤与血液循环阻隔,从而闭塞动脉瘤。该类治疗方法包括:单纯弹簧圈动脉瘤栓塞术、支架辅助弹簧圈动脉瘤栓塞术、球囊辅助弹簧圈动脉瘤栓塞术。
在我国,颅内弹簧圈属于Ⅲ类医疗器械管理,需要进行临床评价。国家药品监督管理局医疗器械技术审评中心推荐的临床评价路径为同品种。
基于《医疗器械分类目录》子目录“13无源植入器械”临床评价推荐路径:
在开展颅内弹簧圈同品种临床评价,论述产品在其适用范围内的安全性和有效性时,应当遵循《关于发布医疗器械临床评价技术指导原则等5项技术指导原则的通告》(2021年第73号),同时结合产品自身特点考虑以下要素:
1)选择适宜的临床评价路径;
根据申报产品是否属于新型医疗器械,是否有前代产品、境外临床数据等,选择适宜的临床评价路径;如果申报产品是新型医疗器械,原则上需要进行临床试验;如果申报产品有前代产品和境外临床数据,对临床评价有很大助益。
2)慎重选择同品种医疗器械;
目前我国已注册的颅内弹簧圈有38款,厂家有史赛克、美敦力、强生、美科微先公司、沛嘉医疗、微创神通、维心医疗、通桥医疗、沃比医疗、加奇生物、秦杰伟业、南京思迈德等。已上市产品的弹簧圈材料均为铂钨合金,部分含有纤毛丝、膨胀丝、凝胶芯。解脱方式主要有电解脱、机械解脱、热解脱等。在选择同品种医疗器械时,应当选择适用范围相同、技术特征和生物学特性相似的同类产品。应综合考量产品的材料,结构组成,规格型号,解脱方式等方面的等同性。在进行等同论证时,需充分收集同品种医疗器械的信息。性能参数的获取是同品种临床评价的共性难题,我们既往经验可以从专利、公开文献、审评报告等官方途径多渠道收集。
3)同品种医疗器械临床数据的数量、适宜性和贡献度;
同品种医疗器械的临床数据包括临床文献数据、临床试验数据和临床经验数据,应综合考虑其临床数据的数量、适宜性和贡献度。建议选择国内外上市,上市时间较长,有丰富临床数据的同类产品。
4)临床前验证的充分性;
一般来说,通过同品种临床评价途径的申报产品缺乏临床试验数据,因此,临床前验证数据需要充分验证临床相关的安全性和有效性。举个例子,动物实验作为医疗器械安全有效性的设计确认主要方式之一,同时也可作为等同论证的重要支持性证据。在动物实验方案设计环节就应充分考量实验的目的,需要验证的指标等。
根据公开资料,神经介入产品已经在全国范围内进行了多轮带量集采,例如,河北省、江苏省和福建省开展的弹簧圈集采等。我司在神经介入领域有着丰富的临床评价经验,按照最小负担原则,助力企业对产品进行临床评价,尽早获批上市。
凌仕医疗
凌仕医疗(LINKS CRO) 是一家专注于创新、高风险、植(介)入医疗器械临床试验的CRO公司,为企业在医疗器械研发过程中提供全过程、一站式的临床试验解决方案。LINKS总部位于上海,下设北、上、广、深分公司及十个办事处。现有员工近200人,其中技术人员超85%,分布于全国近30个城市。
主要业务范围:CRO服务、SMO服务、CER服务、稽查服务、上市后研究、海内外注册、核心实验室、创新申报、国家局答辩辅导、海外企业代理人服务等。
主要治疗领域:心脏领域、神经血管领域、外周血管领域、手术系统领域、肿瘤、眼科、医疗美容,以及其他领域如骨科等,每年提供近300个项目咨询/顾问服务。
